Bạn đang xem: Giải bài tập hóa 10 trang 18 kết nối tri thức
Bài 1: Theo số liệu ở bảng 1 bài bác 1:
a) Hãy tính cân nặng g của nguyên tử nitơ (gồm 7 proton, 7 nơtron, 7 electron) (Đây là phép tính sát đúng).
b) Tính tỉ số khối lượng của electron trong nguyên tử so với khôi lượng của toàn nguyên tử.
Trả lời: a) Tổng cân nặng của proton :
7 x 1,6726.10 –27 = 11,7082.10 –27 kg
Tổng trọng lượng của nơtron :
7 x 1,6748.10 –27 = 11,7236.10-27 kg
Tổng trọng lượng của electron:
7 x 9,1094.10 –31 = 0,0064.10 –27 kg
Khối lượng của nguyên tử nitơ là : 11,7082.10 –27 kg + 11,7236.10-27 kg + 0,0064.10 –27 kg = 23,4382.10 –27 kg.
b) Tỉ số khối lượng của electron vào nguyên tử N và khối lượng của toàn nguyên tử:
Advertisements (Quảng cáo)
Khối lượng các electron/ khối lượng nguyên tử N = 0,0064.10 –27 kg/ 23,4382.10 –27 kg=0,00027 = 0,027%.
Bài 2. (Trang 18 Hóa 10) Tính nguyên tử khối vừa phải của kali hiểu được trong thoải mái và tự nhiên thành phần % các đồng vị của kali là :93,258% 3919K; 0,012% 4019K và 6,730% 4119K.
Trả lời : Nguyên tử khối vừa đủ của kali (K) là: (39 . 93,258 + 40 . 0,012 + 41 . 6,73) /100 = 39,135.
Lưu ý công dụng ra là được thiết kế tròn
Bài 3: a) Định nghĩa thành phần hoá học.
b) Kí hiệu nguyên tử biểu thị những đặc trưng gì đến nguyên tử một nguyên tô’ hoá học, mang thí dụ với yếu tố kali.
Giải bài bác 3: a) Nguyên đánh hoá học bao hàm các nguyên tử có cùng sô đơn vị điện tích phân tử nhân.
b) Kí hiệu nguyên tử 19 K.
Kí hiệu trên mang lại ta biết: Số hiệu nguyên tử của yếu tắc K là 19, số đơn vị điện tích phân tử nhân nguyên tử là 19, trong phân tử nhân có 19 proton với (39 – 19 = 20) nơtron. Vỏ electron của nguyên tử K có 19 electron.
Nguyên tử khối của K là 39u.
Bài 4: Căn cứ vào đâu mà người ta biết chắc chắn là rằng giữa nguyên tố hiđro (Z = 1) với nguyên tố urani (Z = 92) chỉ tất cả 90 nguyên tố.
Từ H bao gồm z = 1, urani tất cả z = 92 có toàn bộ 92 nguyên tố vì số hiệu của những ô trong bảng tuần hoàn là một trong dãy số thoải mái và tự nhiên và không tồn tại ô trông giữa những số thứ tự. Vậy trừ H và urani chỉ từ 90 nhân tố ở khoảng tầm giữa 2 nguyên tố.
Bài 5 Hóa 10 trang 18: Tính bán kính gần đúng của nguyên tử canxi biết thể tích của một mol canxi tinh thể bởi 25,87cm3.
(Cho biết: vào tinh thể, các nguyên tử canxi chỉ chiếm 74% thể tích, sót lại là khe trống).
Đáp án bài 5: Vì trong tinh thể nguyên tử Ca chỉ chiếm khoảng 74% thể tích sót lại là khe trống đề nghị thể tích thực của một mol nguyên tử Ca là: 25,87 . 0,74 = 19,15 (cm3)
1 mol nguyên tử Ca bao gồm chứa 6,022.1023 nguyên tử phải thể tích của một nguyên tử Ca là
Vnguyên tử canxi = 19,15/6,022.1023 ≈ 3.10-23 cm3
Nếu xem nguyên tử Ca là một ủa cầu thì nó có bán kính là
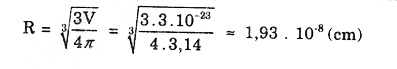
Bài 6 trang 18: Viết công thức của các loại phân tử đồng (II) oxit, hiểu được đồng và oxi có những đồng vị sau :6529Cu , 6329Cu ; 168O , 178O , 188O
a) Hãy tính cân nặng (g) của nguyên tử nitơ (gồm 7 proton, 7 nơtron, 7 electron).
(Đây là phép tính ngay gần đúng).
b) Tính tỉ số cân nặng của electron vào nguyên tử so với trọng lượng của toàn nguyên tử.
(eqalign & m_e = 9,1.10^ - 31,kg = 9,1.10^ - 28,g cr & m_p = 1,67.10^ - 27kg = 1,67.10^ - 24g cr & m_n = 1,675.10^ - 27kg = 1,675.10^ - 24g cr )
a)
Tổng trọng lượng của electron:
7 x 9,1.10 -28 = 63,7.10 -28 g
Tổng cân nặng của proton :
7 x 1,67.10 -24 = 11,69.10 -24 g
Tổng khối lượng của nơtron :
7 x 1,675.10 -24 = 11,72.10-24g
Khối lượng của nguyên tử nitơ là : 23,42.10 -24 g.
Xem thêm: Lý Thuyết Lịch Sử 11 Bài 3 : Trung Quốc, Lịch Sử 11 Bài 3: Trung Quốc
b) (dfrac63,7.10^ - 28 23,42.10^ - 24.100\% approx 0,027\% )
baigiangdienbien.edu.vn


Chia sẻ
Bình chọn:
4.3 trên 104 phiếu
Bài tiếp theo

Luyện bài bác Tập Trắc nghiệm Hóa lớp 10 - xem ngay
Báo lỗi - Góp ý
 |  |  |  |
 |  |  |  |
TẢI ứng dụng ĐỂ xem OFFLINE


× Báo lỗi góp ý
sự việc em chạm mặt phải là gì ?
Sai chủ yếu tả Giải nặng nề hiểu Giải không đúng Lỗi không giống Hãy viết cụ thể giúp baigiangdienbien.edu.vn
gửi góp ý Hủy quăng quật
× Báo lỗi
Cảm ơn các bạn đã sử dụng baigiangdienbien.edu.vn. Đội ngũ thầy giáo cần cải thiện điều gì để chúng ta cho nội dung bài viết này 5* vậy?
Vui lòng nhằm lại tin tức để ad có thể liên hệ với em nhé!
Họ với tên:
gởi Hủy vứt
Liên hệ chính sách







Đăng ký để nhận lời giải hay cùng tài liệu miễn phí
Cho phép baigiangdienbien.edu.vn giữ hộ các thông báo đến các bạn để nhận ra các giải mã hay cũng như tài liệu miễn phí.