Tài liệu Giáo viên
Lớp 2Lớp 2 - liên kết tri thức
Lớp 2 - Chân trời sáng tạo
Lớp 2 - Cánh diều
Tài liệu Giáo viên
Lớp 3Lớp 3 - kết nối tri thức
Lớp 3 - Chân trời sáng sủa tạo
Lớp 3 - Cánh diều
Tài liệu Giáo viên
Lớp 4Sách giáo khoa
Sách/Vở bài xích tập
Tài liệu Giáo viên
Lớp 5Sách giáo khoa
Sách/Vở bài tập
Tài liệu Giáo viên
Lớp 6Lớp 6 - kết nối tri thức
Lớp 6 - Chân trời sáng tạo
Lớp 6 - Cánh diều
Sách/Vở bài xích tập
Tài liệu Giáo viên
Lớp 7Lớp 7 - liên kết tri thức
Lớp 7 - Chân trời sáng tạo
Lớp 7 - Cánh diều
Sách/Vở bài tập
Tài liệu Giáo viên
Lớp 8Sách giáo khoa
Sách/Vở bài xích tập
Tài liệu Giáo viên
Lớp 9Sách giáo khoa
Sách/Vở bài tập
Tài liệu Giáo viên
Lớp 10Lớp 10 - liên kết tri thức
Lớp 10 - Chân trời sáng tạo
Lớp 10 - Cánh diều
Sách/Vở bài tập
Tài liệu Giáo viên
Lớp 11Sách giáo khoa
Sách/Vở bài xích tập
Tài liệu Giáo viên
Lớp 12Sách giáo khoa
Sách/Vở bài tập
Tài liệu Giáo viên
cô giáoLớp 1
Lớp 2
Lớp 3
Lớp 4
Lớp 5
Lớp 6
Lớp 7
Lớp 8
Lớp 9
Lớp 10
Lớp 11
Lớp 12

Để học giỏi Hóa học lớp 9, loạt bài Giải Vở bài xích tập hóa học 9 xuất xắc nhất, cụ thể được biên soạn bám sát đít sgk Vở bài xích tập hóa học lớp 9.
Bạn đang xem: ✅ giải vở bài tập hóa học 9 hay
Mục lục Giải Vở bài xích tập chất hóa học 9
Vở bài xích tập Hóa 9 Chương 1: các loại hợp chất vô cơ
Vở bài xích tập Hóa 9 Chương 2: Kim loại
Vở bài xích tập Hóa 9 Chương 3: Phi kim. Sơ sài về bảng tuần hoàn các nguyên tố hóa học
Vở bài tập Hóa 9 Chương 4: Hiđrocacbon. Nhiên liệu
Vở bài xích tập Hóa 9 Chương 5: Dẫn xuất của Hiđrocacbon. Polime
43 bài bác giảng chất hóa học lớp 9 - Cô Phạm Huyền (Giáo viên Viet
Jack)
Tham khảo tư liệu học xuất sắc môn hóa học lớp 9 hay khác:
Đã có giải mã bài tập môn chất hóa học 10 sách mới:
Trang trước
Trang sau
Học cùng Viet
Jack

Trang web chia sẻ nội dung miễn mức giá dành cho tất cả những người Việt.
Lớp 1-2-3 Lớp 4 Lớp 5 Lớp 6 Lớp 7 Lớp 8 Lớp 9 Lớp 10 Lớp 11 Lớp 12 Lập trình Tiếng Anh
Chính sách bảo mật
Hình thức thanh toán
Chính sách dùng thử đổi mới khóa học
Chính sách hủy khóa học
Tuyển dụng
Tầng 2, số công ty 541 Vũ Tông Phan, Phường Khương Đình, Quận Thanh Xuân, thành phố Hà Nội, Việt Nam
gmail.com


Người đại diện: Nguyễn Thanh Tuyền
Vở bài xích tập chất hóa học lớp 9 - Giải vở bài xích tập hóa học 9 hay, ngắn nhất
Tuyển tập những bài giải vở bài tập chất hóa học lớp 9 hay, ngắn nhất, cụ thể được biên soạn bám quá sát nội dung giấy tờ bài tập hóa học 9 giúp bạn củng vắt kiến thức, biết phương pháp làm bài tập môn hóa học lớp 9.

Chương 1: những loại hợp hóa học vô cơ
Chương 2: Kim loại
Chương 3: Phi kim. Sơ sài về bảng tuần hoàn các nguyên tố hóa học
Chương 4: Hiđrocacbon. Nhiên liệu
Chương 5: Dẫn xuất của Hiđrocacbon. Polime
Vở bài tập hóa học 9 bài xích 1: đặc điểm hóa học tập của oxit. Khái quát về sự việc phân một số loại oxit
I. TÍNH CHẤT HOÁ HỌC CỦA OXIT
1. Oxit bazơ: Oxit bazơ có những đặc thù hóa học nào ?
a) một trong những oxit bazơ công dụng với nước sinh sản thành dung dịch bazơ (kiềm).


II. KHÁI QUÁT VỀ SỰ PHÂN LOẠI OXIT
1. Oxit bazơ là gần như oxit tính năng với hỗn hợp axit chế tạo thành muối và nước.
2. Oxit axit là phần nhiều oxit tác dụng với dung dich bazơ chế tác thành muối cùng nước.
3. Oxit lưỡng tính là hồ hết oxit tính năng với dung dịch axit và tác dụng với hỗn hợp bazơ tạo thành muối và nước.
Ví dụ: Al2O3, Zn
O,...
4. Oxit trung tính (oxit không tạo ra muối) là mọi oxit ko tác dung cùng với axit, bazơ, nước.
Ví dụ: teo
Bài 1. (Trang 6 Vở bài bác Tập hóa học 9 ) bao gồm oxit sau: Ca
O, Fe2O3, SO3. Oxit nào có thể chức năng được với
a) Nước ?
b) axit clohiđric ?
c) natri hiđroxit ?
Viết phương trình hóa học.

Bài 2. (Trang 6 Vở bài xích Tập chất hóa học 9) bao hàm chất sau:
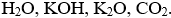
Lời giải:

Bài 3. (Trang 6 Vở bài xích Tập hóa học 9) Từ phần đông chất: canxi oxit, sulfur đioxit, cacbon đioxit, sulfur trioxit, kẽm oxit, em hãy lựa chọn chất phù hợp điền vào những sơ trang bị phản ứng sau:
a) Axit sunfuric + ... → Kẽm sunfat + Nước
b) Natri hiđroxit + ... → Natri sunfat + Nước
c) Nước + ... → Axit sunfurơ
d) Nước + ... → canxi hiđroxit
e) canxi oxit + ... → canxi cacbonat
Dùng các công thức hóa học nhằm viết toàn bộ những phương trình hóa học của những sơ thứ phản ứng trên.
Lời giải:
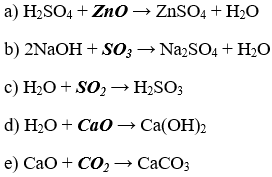
Bài 4. (Trang 6 Vở bài Tập chất hóa học 9) Cho đều oxit sau: CO2, SO2, Na2O, Ca
O, Cu
O. Nên chọn những hóa học đã cho chức năng được với
a) Nước, tạo thành hỗn hợp axit
b) Nước, tạo thành dung dịch bazơ
c) dung dịch axit, tạo ra thành muối với nước.
d) dung dịch bazơ, chế tạo thành muối cùng nước.
Viết các phương trình hóa học.
Lời giải:
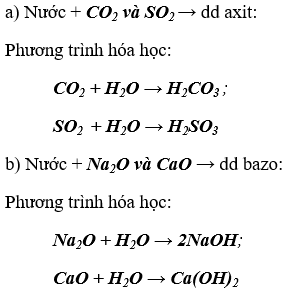

Bài 5. (Trang 6 Vở bài Tập chất hóa học 9) Có hỗn hợp khí CO2 với O2 làm thế nào hoàn toàn có thể thu được khí O2 từ hỗn hợp trên? trình bày cách làm cho và viết phương trình hóa học.
Lời giải:
Cách thu khí O2 từ tất cả hổn hợp O2 và CO2 : Dẫn tất cả hổn hợp khí đi qua dung dịch Ca(OH)2 dư khí CO2 bị hấp thụ hết do có phản ứng cùng với kiềm. Khí thoát thoát khỏi bình chỉ tất cả O2
Phương trình hóa học: CO2 + Ca(OH)2 → H2O + Ca
CO3
Bài 6. (Trang 6 Vở bài Tập hóa học 9) Cho 1,6 gam đồng (II) oxit tính năng với 100 gam dung dịch axit sunfuric có nồng độ 20%.
a) Viết phương trình hóa học.
b) Tính nồng độ tỷ lệ của những chất bao gồm dung dịch sau thời điểm phản ứng kết thúc.
Lời giải:
a) Phương trình hóa học: Cu
O + H2SO4 → Cu
SO4 + H2O
b) Nồng độ xác suất các hóa học trong dung dịch: 0,18 mol H2SO4 cùng 0,02 mol Cu
SO4
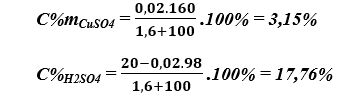
Bài 1. (Trang 7 Vở bài bác Tập hóa học 9) Lưu huỳnh đioxit (SO2) công dụng được với:
A. Nước, sản phẩm là bazo.
B. Axit, thành phầm là bazo.
C. Nước, thành phầm là axit.
D. Bazo, thành phầm là axit.
Lời giải:
Kết quả đúng: C
Oxit axit chức năng với nước tạo ra thành axit
Bài 2. (Trang 7 Vở bài xích Tập hóa học 9) 0,05 mol Na2O tác dụng vừa đầy đủ với:
A. 0,02 mol HCl.
B. 0,1 mol HCl.
C. 0,02 mol Ca
O.
D. 0,01 mol Ca
O.
Lời giải:
Kết quả đúng: B
Phương trình hóa học:
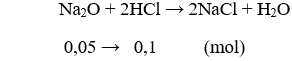
Vậy 0,05 mol Na2O chức năng vừa đủ với 0,1 mol HCl
Bài 3. (Trang 7 Vở bài bác Tập hóa học 9) Đồng (II) oxit (Cu
O) chức năng được với:
A. Nước, thành phầm là axit.
B. Nước, sản phẩm là bazo.
C. Axit, thành phầm là muối với nước.
D. Bazo, thành phầm là muối và nước.
Lời giải:
Kết trái đúng: C
Cu
O + 2HCl → Cu
Cl2 + 2H2O
Vở bài xích tập hóa học 9 bài 2: một số trong những oxit quan lại trọng: canxi Oxit
I. Can xi OXIT CÓ NHỮNG TÍNH CHẤT NÀO ?
Canxi oxit là hóa học rắn , màu sắc white , rét chảy sinh sống ánh sáng rất cao.
Canxi oxit có đầy đủ tính chất của oxit bazo .
1. Chức năng mạnh với nước thành phầm là bazo (phản ứng lan nhiệt)
Phương trình hóa học: Ca
O + H2O → Ca(OH)2
2. Tính năng mạnh với hỗn hợp axit HCl thành phầm là muối Ca
Cl2 với nước.
Phương trình hóa học: Ca
O + 2HCl → Ca
Cl2 + H2O
3. Tính năng với oxit axit thành phầm là muối.
Phương trình hóa học: Ca
O + CO2 → Ca
CO3
Kết luận về đặc thù hóa học của can xi oxit: can xi oxit là oxit bazo.
II. Canxi OXIT CÓ NHỮNG ỨNG DỤNG GÌ?
- phần lớn canxi oxit được dùng trong công nghiệp luyện kim và làm nguyên vật liệu cho công nghiệp hóa học.
- canxi oxit còn được dùng làm khử chua khu đất trồng trọt, xử lý nước thải công nghiệp, gần cạnh trùng, khử nấm, khử độc môi trường,…
- can xi oxit bao gồm tính hút ẩm mạnh đề nghị được dùng để gia công khô nhiều chất.
III. SẢN XUẤT canxi OXIT NHƯ THẾ NÀO?
Sản xuất canxi oxit vào công nghiệp
1. Nguyên liệu: đá vôi (chứa Ca
CO3). Chất đốt là than đá, củi, dầu, khí từ nhiên,…
2. Các phương trình hóa học:
- Than cháy có mặt khí CO2 với tỏa các nhiệt: C + O2 → CO2
- Nhiệt hiện ra phân diệt đá vôi ở khoảng trên 900˚C: Ca
CO3 → Ca
O + CO2
I. Can xi OXIT CÓ NHỮNG TÍNH CHẤT NÀO ?
Canxi oxit là hóa học rắn , color trắng , rét chảy sống ánh nắng mặt trời rất cao.
Canxi oxit có không hề thiếu tính hóa học của oxit bazo .
1. Tác dụng mạnh với nước thành phầm là bazo (phản ứng tỏa nhiệt)
Phương trình hóa học: Ca
O + H2O → Ca(OH)2
2. Tác dụng mạnh với dung dịch axit HCl thành phầm là muối bột Ca
Cl2 cùng nước.
Phương trình hóa học: Ca
O + 2HCl → Ca
Cl2 + H2O
3. Tính năng với oxit axit thành phầm là muối.
Phương trình hóa học: Ca
O + CO2 → Ca
CO3
Kết luận về đặc thù hóa học tập của can xi oxit: can xi oxit là oxit bazo.
II. Can xi OXIT CÓ NHỮNG ỨNG DỤNG GÌ?
- phần lớn canxi oxit được sử dụng trong công nghiệp luyện kim cùng làm vật liệu cho công nghiệp hóa học.
- canxi oxit còn được dùng để khử chua khu đất trồng trọt, up load nước thải công nghiệp, gần kề trùng, diệt nấm, khử độc môi trường,…
- can xi oxit tất cả tính hút ẩm mạnh cần được dùng để gia công khô các chất.
III. SẢN XUẤT can xi OXIT NHƯ THẾ NÀO?
Sản xuất can xi oxit trong công nghiệp
1. Nguyên liệu: đá vôi (chứa Ca
CO3). Chất đốt là than đá, củi, dầu, khí tự nhiên,…
2. Những phương trình hóa học:
- Than cháy có mặt khí CO2 với tỏa các nhiệt: C + O2 → CO2
- Nhiệt ra đời phân bỏ đá vôi ở khoảng chừng trên 900˚C: Ca
CO3 → Ca
O + CO2
Bài 1. (Trang 8 Vở bài bác Tập hóa học 9 ) Bằng cách thức hóa học tập nào hoàn toàn có thể nhận biết được từng chất trong những dãy chất sau ?
a) Hai hóa học rắn white color là Ca
O và Na2O.
b) Hai hóa học khí ko màu là CO2 cùng O2.
Lời giải:
a) nhận ra hai chất rắn Ca
O với Na2O : Hòa chảy 2 hóa học vào 2 ly nước, lọc rước dung dịch, kế tiếp dẫn khí CO2 qua mỗi dung dịch. Dung dịch nào xuất hiện kết tủa (Ca(OH)2) thì thuở đầu là Ca
O
b) phân biệt hai khí O2 và CO2: Cho tàn đóm đỏ vào cụ thể từng khí.Khí nào làm tàn đóm rực rỡ trở lại là khí O2 còn sót lại là CO2
Bài 2. (Trang 8 Vở bài Tập chất hóa học 9 ) Hãy nhận biết từng chất trong những nhóm hóa học sau bằng phương pháp hóa học.
a) Ca
O, Ca
CO3;
b) Ca
O, Mg
O.
Lời giải:
a) nhận ra Ca
O và Ca
CO3 : Cho 2 hóa học vào 2 ông nghiêm cất nước. Ống nào thấy chất rắn rã thì đó là Ca
O
Ca
O + H2O → Ca(OH)2
b) nhận thấy Ca
O và Mg
O: Cho 2 hóa học vào 2 ông nghiêm chứa nước. Ống nào thấy chất rắn tan thì sẽ là Ca
O
Ca
O + H2O → Ca(OH)2
Bài 3. (Trang 9 Vở bài bác Tập hóa học 9 ) 200ml hỗn hợp HCl bao gồm nồng độ 3,5M kết hợp vừa hết trăng tròn g tất cả hổn hợp hai oxit Cu
O và Fe2O3
a) Viết các phương trình hóa học
b) Tính trọng lượng của từng oxit gồm trong các thành phần hỗn hợp ban đầu.
Lời giải:
a) các phương trình hóa học:
Cu
O + 2HCl → Cu
Cl2 + H2O (1)
Fe2O3 + 6HCl → 2Fe
Cl3 + 3H2O (2)
Khối lượng của từng oxit trong lếu láo hợp: x + y = 20; n
HCl = 3,5.0,2 = 0,7 mol
Gọi trọng lượng của Cu
O trong hỗn hợp là x và Fe2O3 là y (gam).
Từ (1) với (2) ta có:
x + y = 20
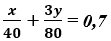
Giải hệ phương trình ta được x = 4 gam với y = 16 gam.
Bài 4. (Trang 9 Vở bài xích Tập chất hóa học 9 ) Biết 2,24 lít khí CO2 (đktc) công dụng vừa không còn với 200 ml hỗn hợp Ba(OH)2 thành phầm là Ba
CO3 và H2O
a) Viết phương trình hóa học
b) Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng
c) Tính khối lượng chất kết tủa thu được.
Lời giải:
a) Phương trình hóa học: CO2 + Ba(OH)2 → Ba
CO3 + H2O
b) mật độ mol của dung dịch Ba(OH)2 :
n
CO2 = 0,1mol
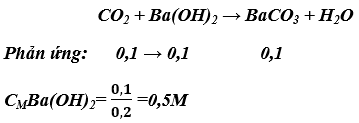
c) khối lượng kết tủa :
Chất kết tủa chiếm được sau phản ứng là Ba
CO3 bao gồm số mol là 0,1
m
Ba
CO3 = 0,1 × 197 = 19,7g
Bài 1. (Trang 9 Vở bài bác Tập chất hóa học 9) Sản xuất vôi sinh sống Ca
O bằng phương pháp nung đá vôi (thành phần chính là canxi cacbonat Ca
CO3).
a) Viết phương trình hóa học.
b) từ 1 tấn đá vôi bao gồm chứa 80% canxi cacbonat hoàn toàn có thể sản xuất được từng nào tấn vôi sống?
Lời giải:
a) Phương trình hóa học: Ca
CO3 → Ca
O + CO2
b) khối lượng vôi sống tiếp tế được:
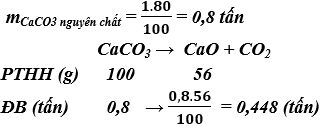
Bài 2. (Trang 9 Vở bài xích Tập chất hóa học 9) Hãy tiến hành các phân tích để đào thải tạp chất thoát khỏi hỗn phù hợp sau:
a) Khí O2 lẫn tạp hóa học là CO2.
b) không khí (hỗn hợp N2 và O2) tất cả lẫn tạp chất là SO2.
c) Bột Ca
CO3 bao gồm lẫn tạp chất là Ca
O.
Lời giải:
a) thải trừ tạp hóa học CO2 lẫn với O2 : Dẫn các thành phần hỗn hợp qua hỗn hợp nước vôi vào Ca(OH)2 . CO2 phản nghịch ứng cùng với Ca(OH)2 tạo ra kết tủa trắng cùng bị cất giữ trong dung dịch.
Phương trình hóa học: Ca(OH)2 + CO2 → Ca
CO3 + H2O
b) loại trừ tạp chất SO2 tất cả trong không khí: Dẫn hỗn hợp qua hỗn hợp nước vôi vào Ca(OH)2 . SO2 phản bội ứng cùng với Ca(OH)2 tạo kết tủa trắng cùng bị cất giữ trong dung dịch.
Phương trình hóa học: Ca(OH)2 + SO2 → Ca
SO3 + H2O
c) thải trừ tạp chất Ca
O khỏi Ca
CO3: Ca
O tính năng với CO2 tạo nên thành Ca
CO3
Phương trình hóa học: Ca
O + CO2⟶ Ca
CO3
Bài 3. (Trang 9 Vở bài bác Tập hóa học 9) Khối lượng Ca(OH)2 tiếp tế được từ 112kg Ca
O tác dụng với H2O là
A. 74 kilogam B. 148 kilogam C. 14,8 kilogam D. 7,4 kg
Lời giải:
Kết trái đúng: B
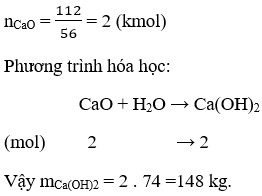
Vở bài xích tập chất hóa học 9 bài bác 2: một số trong những oxit quan lại trọng: diêm sinh Đioxit
I. LƯU HUỲNH ĐIOXIT CÓ NHỮNG TÍNH CHẤT GÌ?
Lưu huỳnh Đioxit là chất khí không màu, mùi hương hắc, độc (gây ho, viêm mặt đường hô hấp…), nặng rộng không khí.
II. LƯU HUỲNH ĐIOXIT CÓ NHỮNG ỨNG DỤNG GÌ?
- đa số SO2 dùng làm sản xuất axit sunfuric H2SO4.
- sử dụng làm chất tẩy white bột mộc trong tiếp tế giấy, đường,…
- cần sử dụng làm chất diệt nấm mốc,…
III. ĐIỀU CHẾ LƯU HUỲNH ĐIOXIT NHƯ THẾ NÀO?
1. Trong phòng thí nghiệm: mang đến muối sunfit khi công dụng với axit mạnh dạn như HCl, H2SO4,…
Phương trình hóa học: Na2SO3(tt) + H2SO4 → Na2SO4 + SO2 + H2O
2. Trong công nghiệp: Đốt lưu hoàng hoặc quặng pirit fe Fe
S2 trong không khí:
S + O2 → SO2
4Fe
S2 + 11O2 → 2Fe2O3 + 8SO2
Bài 1. (Trang 11 Vở bài Tập chất hóa học 9 ) Viết phương trình hóa học đến mỗi biến đổi
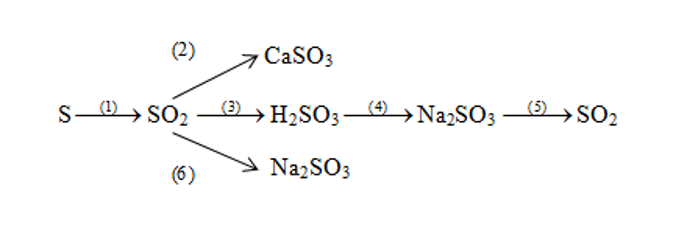
Lời giải:
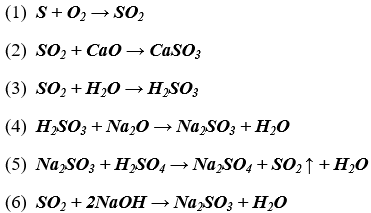
Bài 2. (Trang 11 Vở bài xích Tập chất hóa học 9 ) Hãy phân biệt từng chất trong những nhóm chất sau bằng phương pháp hóa học
a) Hai chất rắn màu trắng là Ca
O cùng P2O5
b) Hai hóa học khí ko màu là SO2 và O2
Lời giải:
Nhận biết các chất:
a) Ca
O với P2O5: chan nước vào nhì ống nghiệm gồm chứa Ca
O cùng P2O5. Tiếp nối cho quỳ tím vào từng dung dịch. Qùy tím chuyển xanh thì chất ban đầu là Ca
O, còn lại chuyển đỏ là P2O5
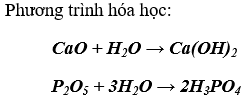
b) SO2 và O2 : Dẫn theo thứ tự từng khí vào dung dịch nước vôi trong, nếu gồm kết tủa xuất hiện thêm thì khí đem vào là SO2.
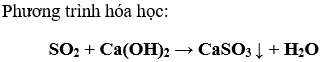
Bài 3. (Trang 11 Vở bài bác Tập chất hóa học 9 ) gồm có khí ẩm (khí tất cả lần khá nước): cacbon đioxit, hiđro, oxi, diêm sinh đioxit. Khí nào hoàn toàn có thể được làm cho khô bằng canxi oxit? Giải thích.
Lời giải:
Ca
O có thể được dùng để làm khô những khí (bị ẩm) sau : H2, O2
Giải thích: Ca
O chỉ có tác dụng khô hầu hết chất không tồn tại phản ứng chất hóa học với Ca
O, kia là các chất H2, O2.
Bài 4. (Trang 11 Vở bài xích Tập chất hóa học 9 ) bao hàm chất khí sau: CO2, H2, O2, SO2, N2. Hãy cho biết chất như thế nào có đặc điểm sau:
a) nặng hơn không khí.
b) khối lượng nhẹ hơn không khí
c) cháy được trong ko khí.
d) công dụng với nước sản xuất thành dung dịch axit
e) làm cho đục nước vôi trong
g) thay đổi màu giấy quỳ tím độ ẩm thành đỏ.
Lời giải:
a) Nặng hơn không khí: CO2 , O2, SO2
b) nhẹ hơn không khí: H2 , N2
c) Cháy được trong không khí: H2
d) công dụng với nước sản xuất thành hỗn hợp axit: CO2, SO2
e) có tác dụng đục nước vôi trong : CO2, SO2
g) Đổi color giấy quỳ tím ẩm thành đỏ : CO2, SO2
Bài 5. (Trang 12 Vở bài Tập chất hóa học 9 ) Khí lưu huỳnh đioxit được sản xuất thành từ bỏ cặp hóa học nào tiếp sau đây ?
a) K2SO3 và H2SO4.
b) K2SO4 và HCl.
c) Na2SO3 với Na
OH
d) Na2SO4 và Cu
Cl2.
e) Na2SO3 cùng Na
Cl.
Lời giải:
Khí SO2 được tạo ra thành tự cặp chất: K2SO3 với H2SO4
Phương trình hóa học: K2SO3 + H2SO4 → K2SO4 + SO2 ↑ + H2O
Bài 6. (Trang 12 Vở bài bác Tập chất hóa học 9 ) Dẫn 112 ml khí SO2 (đktc) đi qua 700 ml dung dịch Ca(OH)2 tất cả nồng độ 0,01 M, sản phẩm là muối can xi sunfit.
Xem thêm: Giải Bài Tập Địa Lý Lớp 7 Bài 17 : Ô Nhiễm Môi Trường Ở Đới Ôn Hòa
a) Viết phương trình hóa học
b) Tính khối lượng các hóa học sau phản ứng.
Lời giải:
a) Phương trình bội phản ứng hóa học: SO2 + Ca(OH)2 → Ca
SO3 + H2O
b) khối lượng các hóa học sau phản ứng:
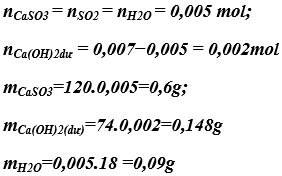
Bài 1. (Trang 12 Vở bài Tập chất hóa học 9) Có đầy đủ chất sau: H2O, SO3, Na2O, KOH, Fe2O3, Mg
O, P2O5, CO2.
Những chất nào có thể công dụng với nhau từng song một?
Viết các phương trình hóa học.
Lời giải:
Những chất có thể công dụng với nhau từng đôi một:
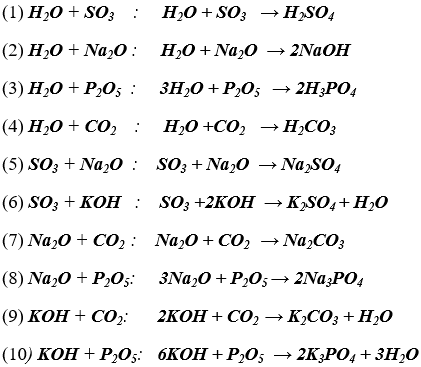
Bài 2. (Trang 12 Vở bài Tập chất hóa học 9) Hãy tiến hành những chuyển đổi sau bằng phương pháp viết những phương trình hóa học: